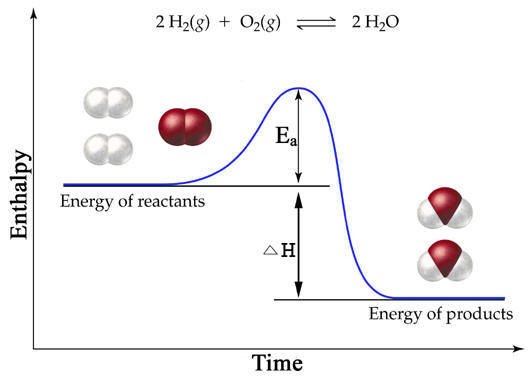
Darüber hinaus sagt uns die Entropie auch die Möglichkeit verschiedener chemischer Prozesse und den Grund für ihre reversible und irreversible Natur.Verschiedene Definitionen von EntropieQuelle: Forschungsarbeit
Entropie wird oft als Verlust an Energie bezeichnet, die zur Verfügung steht, um Arbeit zu verrichten. Sie wird auch mit der Tendenz zur Unordnung in einem geschlossenen System in Verbindung gebracht.
Entropie wird für die quantitative Analyse von verwendet
Zweiter Hauptsatz der Thermodynamik

Je mehr Energie ein System an seine Umgebung verliert, desto ungeordneter und zufälliger wird das System. Hohe Entropie bedeutet hohe Unordnung und niedrige Energie. Wir können die Analogie eines Jugendzimmers verwenden. Wenn keine Energie oder Arbeit vorhanden istEingesetzt wird der Raum schnell unordentlich und unordentlich und hat eine hohe Entropie.Bei Energieeintrag in das System, in Form von Aufräumen und Wegräumen, wird der Raum wieder in einen Ordnungszustand bzw. eine niedrige Entropie gebracht.
WerbungEntropieformeln und GleichungenQuelle:
Kairen Bailey/Unsplash
Es gibt zahlreiche Gleichungen, die die Entropie in Bezug auf verschiedene wissenschaftliche Parameter ableiten. Die für eine Wärmekraftmaschine formulierte Entropiegleichung wird jedoch häufiger verwendet, da sie sowohl den zweiten Hauptsatz der Thermodynamik als auch den Gleichgewichtszustand eines Systems effizient beschreibt describes.
ΔS = Q/T

ΔS = Q 1/T1
- 1/T2
Hier, T1 hat einen höheren Wert als T2WerbungWennT1 = T2, dann gibt es keinen Wärmefluss und das System befindet sich im GleichgewichtNun, wenn es eine Wärmekraftmaschine gibtQ1
Wärmemenge aus einem Reservoir und Q2 Wärmemenge des anderen, dann wäre nach dem Energieerhaltungssatz die vom Motor in einem Zyklus geleistete Arbeit W: W = Q1 - Q2Für ein solches System wird die Entropieänderung berechnet als ΔS = Q2/T2- Q1/T1
Maximale Arbeit ist erledigt, wenn der Wert von Q2 ist sehr klein im Vergleich zu Q1 aber der Wert von Q2 kann nicht Null sein, da in diesem Fall die Entropieänderung negativ ausfällt. Nach dem zweiten Hauptsatz der Thermodynamik ist der kleinstmögliche Wert der Entropieänderung ΔS Null. Werbung
Dann, Q2/Q1min = T2/T1Wenn die Entropieänderung Null ist, findet ein reversibler Vorgang statt, da in einem solchen Fall schon die kleinste Änderung ausreicht, um die Wärmekraftmaschine rückwärts zu laufen.Quelle:
LumenUm die Entropieänderung für ein System wie einen mit einem beweglichen Kolben ausgestatteten Gaszylinder zu bewerten, sei der Gaseinlass dQ Wärmemenge bei einer gegebenen Temperatur T. Wenn also ein entgegengesetzter Rückhaltedruck P angelegt wird,das Gas im Zylinder dehnt sich reversibel um dV Volumen aus, hier wird die maximale Arbeit berechnet als:dW = PdVWenn die Änderung die innere Energie U des Systems während dieses Prozesses ist dU, dann:dQ = dU + PdVUnd die Entropieänderung für das Reservoir wäre:
dSres = −dQ/TWerbungUm nun die Entropieänderung zwischen System und Reservoir auszugleichen, wird die Entropieänderung für das System wie folgt erhöht:
dS
sys = dU + PdV/T dSsys = dQ/T dSsys + dSres = 0. Der Wert der geleisteten Arbeit ist immer geringer als die maximal mögliche Arbeit in einem praktischen Verfahren, da immer einige unvermeidbare Energieverluste aufgrund von Reibung und anderen Gründen auftreten.Im Fall eines im Vakuum frei expandierenden Gases ist die Entropieänderung
dSsys= dU+PdV/T ≥dQ'/THier dQ' = aufgenommene Wärmemenge dQ = maximal mögliche Wärmemenge und wenn dQ'>dQ ist der Prozess reversibel. Diese Entropiegleichung zeigt, dass die Menge des Materials innerhalb eines Systems und sein aktueller Zustand den Entropiewert beeinflussen.WerbungLudwig BoltzmannQuelle: Forschungstor
Wenn ein sehr großes System im thermodynamischen Gleichgewicht existiert, bezeichnet die Größe Ω die Gesamtzahl der dem System zugänglichen Mikrozustände
, dann: S = k ln ΩHier k = Boltzmann-Konstantek = 1,38 ×10-23m2 kg s-2 K-1Entropie wird mit 'S' bezeichnet und seine SI-Einheit ist Joule pro Kelvin JK-1 oder kg m2 kg s-2 K-1Enthalpie vs. EntropieQuelle: CSBSJUStudenten werden oft zwischen Enthalpie und Entropie verwechselt, die zwei völlig verschiedene Teile des thermodynamischen Systems sind. Der grundlegende Unterschied zwischen den beiden besteht darin, dass Entropie S den Grad der Zufälligkeit oder Unordnung innerhalb eines Systems bezeichnet, während Enthalpie Hist die Gesamtwärmemenge, die in einem System bei einem bestimmten Druck vorhanden ist.
WerbungΔS=ΔQ/T
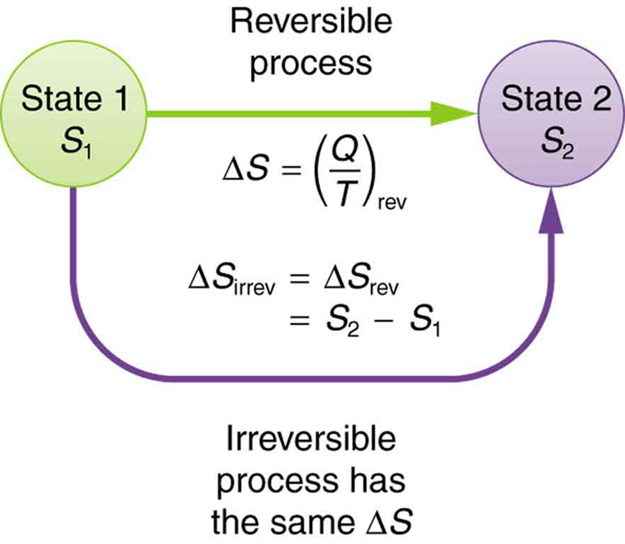
Enthalpieänderung ΔH wird auch als Produkt aus Entropieänderung ΔS und absoluter Temperatur T bezeichnet:
ΔH = T ΔS
Die SI-Einheit der Enthalpie ist J mol−1
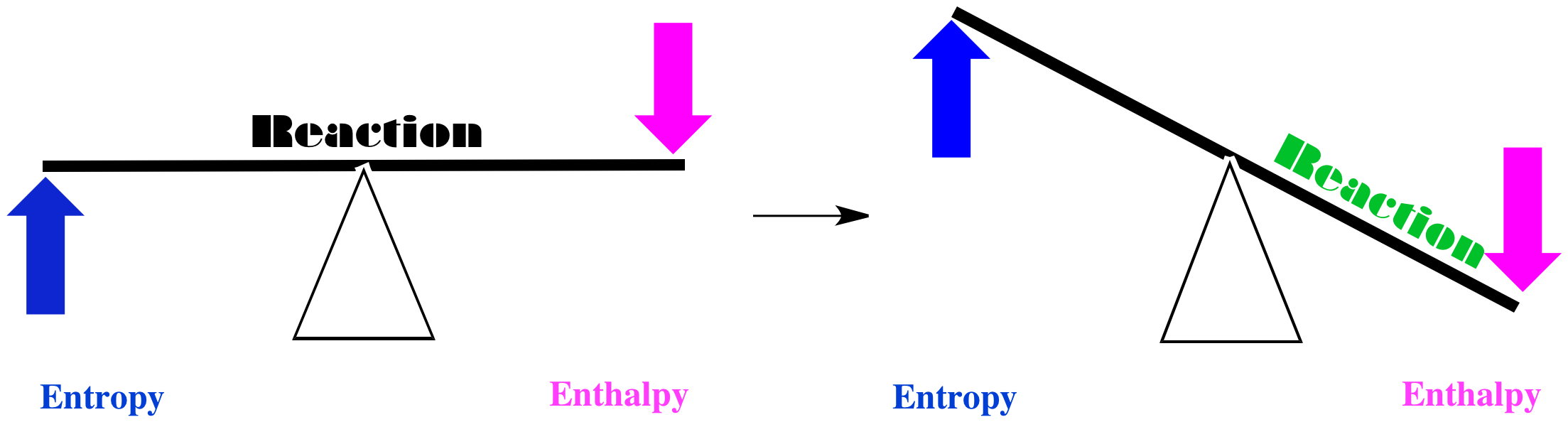
Einige Hauptunterschiede zwischen Enthalpie und Entropie bestehen darin, dass erstere eine von einem System abgeleitete Energieform ist, letztere jedoch eine Eigenschaft des Systems. Darüber hinaus neigt jedes System dazu, Unordnung in seinem Zustand oder seiner molekularen Struktur zu begünstigen, also Entropieist durch keine Bedingungen eingeschränkt, aber Systeme bevorzugen keine Enthalpie, daher ist sie nur anwendbar, wenn Standardbedingungen bereitgestellt werden.
Quelle:
SokratischIm Kontext makroskopischer Systeme, sowohl Entropie als auch Enthalpie gelten als fundamentale Größen, aber unter Berücksichtigung der Quantenmechanik werden diese Größen ableitbar.
Quelle:
Alexander Andrews/UnsplashEntropie ist nicht nur auf Physik und Chemie beschränkt, es gibt verschiedene Anwendungen
dieses Konzepts in Soziologie, Psychologie, Wirtschaft, Philosophie, Biologie, Klimawandel, Informationssysteme und vielen anderen Disziplinen. Dies liegt vor allem daran, dass Zufälligkeit oder Chaos als ein unvermeidlicher Bestandteil fast jedes Prozesses angesehen wird.Ein gemütliches Lagerfeuer, kochendes Wasser, Eis schmelzen, Popcorn kochen und Tee kochen – all diese Aktivitäten sind ein Ergebnis der Entropie,
und sogar das Universum tendiert zu höherer Entropie.Von Menschenhand geschaffene Dinge wie Maschinen, Möbel und Geräte sind weniger entropisch als natürliche Objekte, da sie so gebaut sind, dass sie optimal, konzentriert und organisiert bleiben oder funktionieren.Neuere Forschung zeigt, dass eine Uhr, die die maximale Entropie ausstrahlt, die genaueste Zeit anzeigt.
Das Konzept der Entropie ist auch ein Teil der menschlichen Physiologie und des menschlichen Verhaltens, es kann
beeinflussen Ihre Gesundheit, Beziehungen, Finanzen und viele andere Aspekte Ihres Lebens positiv oder negativ, abhängig von Ihrer Reaktion auf die verschiedenen Ebenen.WerbungFolgen Sie uns auf
Bleiben Sie über die neuesten technischen Nachrichten auf dem Laufenden
Geben Sie einfach Ihre E-Mail ein und wir kümmern uns um den Rest :
ABONNIEREN
Mit der Anmeldung stimmen Sie unseren zu

Gesponserte GeschichtenempfohlenKulturBiomechanik und die Physik des Amputierten-FußballsRaycene Nevils-Karakeci
vor 2 Monaten
WissenschaftIst das Standardmodell der Teilchenphysik wirklich Kaput?Marcia Wendorf
vor 1 MonatWissenschaftJe genauer eine Uhr tickt, desto mehr Entropie gibt sie ab, finden PhysikerDerya Özdemirvor 1 MonatWissenschaftDie überraschend einfache Physik des Doppler-EffektsLoukia Papadopoulosvor 2 MonatenWerbung1457
WerbungINTERESSANTE TECHNIKÜber unsWerbenJobsNewsletterKontaktieren Sie unsKATEGORIENInnovation
WissenschaftDIY
© Copyright 2021 | Interessante Technik | wissenschaft-x.com, Inc. | Alle Rechte vorbehalten
Richtlinien×
Bleib oben
das neueste
Ingenieurnachrichten
Mit der Anmeldung stimmen Sie unseren zu
Nutzungsbedingungen
und